�������ڣ�2018��8��24�� �Ķ���2299
ҽ����е**��ʶ(Unique Device Identification�����UDI)����ҽ����е��Ʒ������֤����������ŷ����أ��ձ����Ĵ����ǡ�����͢�������ȹ���չ���������ҹ�Ҳ�������ճ̡�
2018��8��22�գ������г��ල�����ַܾ����ˡ�ҽ����е**��ʶϵͳ����(���������)��(���¼�ơ���������塷)��������ҽ����е**��ʶϵͳ�������Ҫ��ּ�����ҽ����е�Ŀ����ԣ����������һ���µ�ʱ��(2018��8��22�յ�2018��9��21��)��ҽ����е**��ʶϵͳ������ʽ����!

ʵ������Ρ���������������ǿ�Ѩ���磬�ڽ���2��28�գ�ԭ����ʳƷҩƷ�ල�����ܾ���������ҽ����е**��ʶϵͳ����(���������)���������˵������ͬ����չ��WTO/TBTͨ�������յ����267������������������96������Ҫ����������ض����ҽ����е��Ʒ�ĺϹ桢����ԭ�������ϴ�ʱ��Ҫ�����µ�**��ʶ���Ҫ��ͷ������ȷ�����й����⡣�˴Ρ������������ԭ���Ļ�������ϸ�ˡ�**��ʶϵͳ���塿�����������ˡ�����������͡��������Ҫ�����������ݡ�
ҽе�㽫ҽ����е**��ʶ(UDI)ϵͳ�������£�
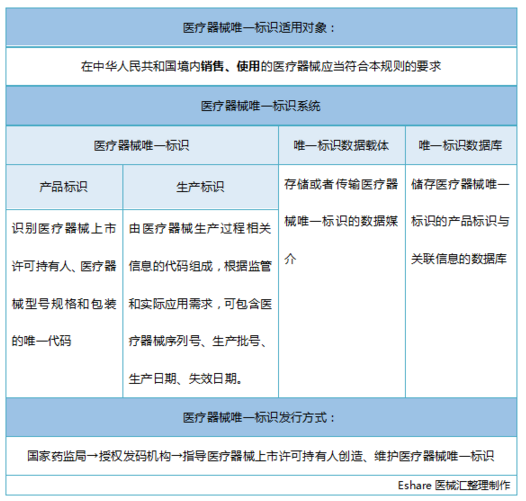
ҽ����е**��ʶ�ǹ���ҽ����е��������ע���ȵ㣬��ȫ��ҽ����е����ֶδ��º�Ч�������ķ�չ����ҽе��Ҳ����������ص�������ŷ�˵�UDI������ݡ�
����
������ҽ����е**��ʶϵͳ��FDA������ּ�ڷ����ʹ�û��ڳ��ʶ��ҽ����е��
���ҹ�ҽ����е�������ɳ�������Ե���������ҽ����е��ǩ�̡���ǩ������ҽ����е������ǩ����б�ǩ�ĵ��ˣ�ּ�ڽ�ҽ����е�����ݼ�ó���У�����������������ı�ǩ����ǩ�̱�����FDA��ȫ��**��е��ʶ���ݿ�(GUDID)�ύÿ���豸���ض���Ϣ��
GUDID��FDA�������������о���**��ʶ��ҽ����е������UDI��ÿ��ҽ����е�ı�ǩ�̱��뽫�йظ��豸����Ϣ�ύ��GUDID�������л�������������
Ŀǰ��FDA��Ȩ������������ֱ��ǣ�GS1��HIBCC��ICCBBA��
ŷ��
Medical Device Directives Revision (2012) Article 24 �涨�ˣ������ƻ�����ʵ���ҽ����е����Ҫʹ��UDIϵͳ��
2012��2�£�Eucomed�����ˡ����ڷ��չ����IJ�ͬ��װ����ҽ����еUDI��ʶҪ�����ļ�����ŷ��ҽ����е����III��IIb��IIa��I����Ӧ������������3��2��1�࣬����˲�ͬ��װ�ȼ���UDI�ı�ʶҪ��
2017��5�£�ŷ�˷���ҽ����е���棬���IMDRFָ�Ϻ�����FDA���棬��ȷ��ŷ��ʵʩҽ����е**��ʶ��Ҫ��
ͨ������UDIϵͳ��������Ϣ�����ֶΣ�ҽԺ֮�䡢����֮�䡢ʡ��֮����ϰ���ȫ����ͨ��ҽ����еȫ����������ݵļ��֮�С����������ܲ��ŵĹ�����������ҵ�����������Ǿ����̵���ͨ���Լ�ҽԺ��ʹ�ö��ܼ�ʱ�����ݿ��еõ������Ե��˽⡣��δ����ҽе�������ڴ��ڵ���Ƥ�ӵ��£�ҽе��ҵֻ��Խ��Խ�Ϲ档
������Դ������ҽҩ��
1.������ע������Դ��1168ҽҩ����������������Ʒ����Ϊ���ݽ��ڻ������Ƽ�����˾-1168ҽҩ�������Ϸ�ӵ�а�Ȩ����Ȩʹ�õ���Ʒ��δ��������Ȩ����ת�ء�ժ�������������ʽʹ��������Ʒ���Ѿ�������Ȩʹ����Ʒ�ģ�Ӧ����Ȩ��Χ��ʹ�ã���ע������Դ��1168ҽҩ������http://www.1168.tv����Υ�����������ߣ�������������ط������Ρ�
2.����ת�ز�ע����������Դ����1168ҽҩ������������Ʒ��Ŀ�����ڴ��ݸ�����Ϣ����������������ͬ��۵��Ͷ�����ʵ�Ը��𣬲��е�������Ʒ��Ȩ��Ϊ��ֱ�����μ��������Ρ�
3.����ý�塢��վ����˴ӱ���ת��ʱ�����뱣������ע������Ʒ��һ��Դ�����Ը���Ȩ�ȷ������Ρ�
4.���漰��Ʒ���ݡ���Ȩ�����⣬������Ʒ����֮����һ�����뱾����ϵ��������Ϊ�������Ȩ������ϵ���䣺1753418380@qq.com��

�����÷�Χ�����ڻ��⾱���硢�����ȼ��պ�������֯��ʹ�����͵Ȳ���֢״��Ⱥ���������ʹ�÷��������á�����Ʒ����ֱ��ͿĨ�ڲ��ʲ�λ�����ᰴĦ2-3���ӣ�ÿ��2-3�Ρ�

�����÷�Χ�����ڻ��⾱���硢�����ȼ��պ�������֯��ʹ�����͵Ȳ���֢״��Ⱥ���������ʹ�÷��������á�����Ʒ����ֱ��ͿĨ�ڲ��ʲ�λ�����ᰴĦ2-3���ӣ�ÿ��2-3�Ρ�
 ���������� 44011102000390��
���������� 44011102000390��